呼吸链与电子传递
在三羧酸循环中,乙酰CoA氧化释放的大部分能量都储存在辅酶(NADH和FADH2)分子中。细胞利用线粒体内膜中一系列的电子载体(呼吸链),伴随着逐步电子传递,将NADH或FADH2进行氧化,逐步收集释放的自由能最后用于ATP的合成,将能量储存在ATP的高能磷酸键。
■ 电子载体(electron carriers)
在电子传递过程中与释放的电子结合并将电子传递下去的物质称为电子载体。参与传递的电子载体有四种∶黄素蛋白、细胞色素、铁硫蛋白和辅酶Q,在这四类电子载体中,除了辅酶Q以外,接受和提供电子的氧化还原中心都是与蛋白相连的辅基。
● 黄素蛋白(flavoproteins) 黄素蛋白是由一条多肽结合1个辅基组成的酶类,每个辅基能够接受和提供两个质子和电子(图7-22)。
● 细胞色素(cytochromes) 细胞色素是含有血红素辅基(图7-24)的一类蛋白质。在氧化还原过程中,血红素基团的铁原子可以传递单个的电子。血红素中的铁通过Fe3+和 Fe2+两种状态的变化传递电子;在还原反应时,铁原子由Fe3+状态转变成Fe2+状态;在氧化反应中,铁由Fe2+转变成Fe3+.
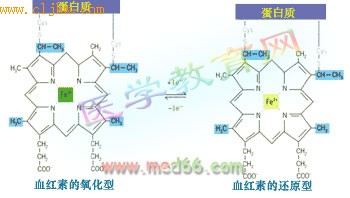
图7-24 细胞色素c的血红素基团的结构及氧化还原状态的变化
四个卟啉环都含有侧链,不同的细胞色素所含侧链不同。图中所示是细胞色素c,血红素与多肽的两个半胱氨酸共价结合,但在大多数细胞色素分子中,血红素并不与多肽共价结合。
● 铁硫蛋白(iron-sulfur proteins, Fe/S protein) 铁硫蛋白是含铁的蛋白质,也是细胞色素类蛋白。在铁硫蛋白分子的中央结合的不是血红素而是铁和硫,称为铁-硫中心(iron-sulfur centers, 图7-25)。

图7-25 两种类型的铁硫蛋白的结构
(a)2Fe-2S型铁硫蛋白; (b)4Fe-4S型铁硫蛋白
醌(uniquinone UQ)或辅酶Q(coenzyme Q) 辅酶Q是一种脂溶性的分子,含有长长的疏水链,由五碳类戊二醇构成。如同黄素蛋白,每一个醌能够接受和提供两个电子和质子(图7-26),部分还原的称为半醌,完全还原的称为全醌(UQH2)。
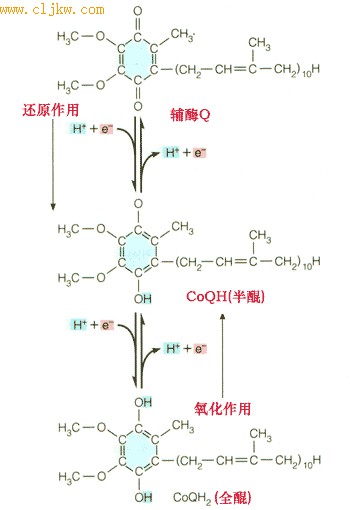
图7-26 辅酶Q的氧化和还原形式
辅酶Q的氧化还原分两步进行,先接受一个电子,得到部分还原,称为半醌,再得到一个电子,成为完全还原的醌,称为全醌。全醌失去一个电子是部分氧化,成为半醌,两个电子全部失去,即完全氧化则称为还原型的醌。
■ 氧化还原电位与载体排列顺序
● 氧还电位(oxidation-reduction potentials, redox potentials)
不同的还原剂具有不同的电子传递电位,而氧化与还原又是偶联的,如NAD+和NADH.它们的差别主要是电子数量不同,所以二者间就有一个电位差,即氧还电位。
● 呼吸链中电子载体的氧还电位
氧还电位在标准条件下测定,即得标准氧化还原电位(standard oxidation reduction potentials, E0')。表7-4 是测得的某些电子载体的标准氧还电位。
表7-4 某些电子载体
[1] [2] [3] 下一页
